摘要
硫羰基叶立德CH2=S(+)−CH2(−)与缺电子环烯烃的[3+2]环加成反应可制得双环硫醚类化合物,该反应在毫克、克乃至数克级反应规模下均能高效进行。对所得产物进行标准修饰,可得到适用于药物化学研究的稠合与螺环砜类化合物。
引言
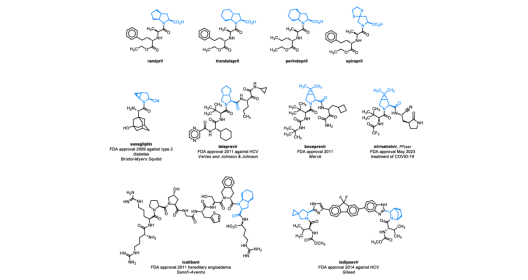
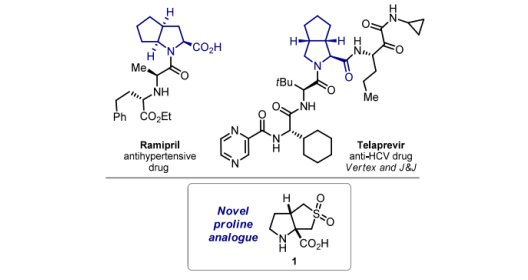
双环脯氨酸是现代药物研发中应用广泛的合成砌块,雷米普利、特拉普韦等药物的结构中均含有该类基团。基于对这类分子的持续研究兴趣,本研究计划合成新型含SO2的双环脯氨酸1(图1)。本文将报道该化合物的合成方法,并阐述关键的[3+2]环加成步骤如何逐步发展为合成药物化学用稠合与螺环砜类化合物的通用方法。
对氨基酸1进行逆合成分析后,我们推测烯烃2可能也能与硫羰基叶立德发生类似反应。1986年,Sakurai课题组发现,硫化物3在氟化铯存在下可生成硫羰基叶立德CH2=S(+)−CH2(−),且该叶立德能与直链缺电子烯烃发生反应。本研究尝试将该反应应用于烯烃2,最终成功实现目标产物的合成。
反应适用范围
砜基是有机合成和药物化学中常见的官能团,基于此,本研究进一步探索了该[3+2]环加成策略在合成其他官能化双环砜类化合物中的应用,分别考察了稠环产物和螺环产物的合成效果,并分析了反应的局限性及解决方法。
稠环产物
环内四元烯烃4~6在室温下可与硫化物3顺利反应,以71%~81%的收率得到产物4a~6a;五元烯烃7和8的反应收率为52%~68%;杂原子取代的五元烯烃9~14也能与3发生反应生成9a~14a,其中钝化烯烃10(含大位阻三氟甲基)和13(推-拉电子型烯烃)的反应速率较慢,需加热并补加试剂才能完成反应;六元及七元烯烃15~18的反应活性最低,产物15a~18a的收率中等,仅为30%~41%。
螺环产物
环外三元及四元烯烃19~28的反应性整体较好,产物19a~28a的收率为52%~94%。值得注意的是,在烯烃片段中引入氟原子(21、24、26)可显著提高其反应活性,促进反应进行;六元烯烃29~32的反应活性较差,螺环四氢噻吩类化合物29a~32a的收率仅为14%~29%。
反应机理
结论
硫羰基叶立德CH2=S(+)−CH2(−)与缺电子环烯烃的[3+2]环加成反应可高效制备稠合与螺环硫醚类化合物。根据起始烯烃的结构差异,可灵活选用硫化物3或亚砜41作为硫羰基叶立德前体进行反应。对所得硫醚产物进行标准的有机合成修饰,能够得到一系列适用于药物化学研究的稠合与螺环砜类化合物,为药物研发提供了新型结构多样的合成砌块。
本文中涉及的含稠合与螺环砜类化合物砌块与相关衍生物,Enamine均有现货供应。